Nos últimos dias falámos várias vezes de alginatos e da sua utilização na alimentação, embora eles tenham uma enorme variedade de aplicações noutras áreas. Sabia que também são usados pelos dentistas para fazer moldes dos dentes?
De facto há material de moldagem usado pelos dentista à base de alginato que consiste num pó, alginato de sódio ou de potássio misturado com sulfato de cálcio, que quando misturado com água forma um gel de fixação rápida. Já lhe tinhamos dito que na presença de cálcio o alginato gelifica, neste processo o cálcio substitui os iões de sódio ou potássio, permitindo a interligação de algumas zonas das cadeias de alginato e resultando na formação de um gel. Os fabricantes adicionam ainda outras substâncias para controlar a consistência, tempo de gelificação, elasticidade, força e estabilidade.
O alginato pode ainda ser usado para fazer moldes de outras partes do corpo, ou de outros objectos. Veja aqui por exemplo a realização de um molde de uma cara:
segunda-feira, 31 de outubro de 2011
domingo, 30 de outubro de 2011
A Química na Arte XXVII
Se puder, não deixe de ir ver!
INVULGAR – que não é vulgar, comum; especial, raro, incomum (Dic. Houassis).
... pois é. FALÁCIA não é um espectáculo qualquer mas, na realidade será um espectáculo INVULGAR!... Invulgar porque não é uma coisa que se veja todos os dias. Invulgar porque talvez nunca mais volte a ter a possibilidade de ver.
Nesta peça – FALÁCIA – há um debate vivo, audacioso e cativante, com sentimentos amorosos a cruzarem-se e a prender o espectador pelo “bico”. Num importante museu europeu, em Viena de Áustria, encontra-se a estátua de um rapaz nu, atribuída à era romana e que é a jóia da coroa do museu. Mas a ciência, através da química, desmistifica aquela era. E o valor artístico da obra, para além da data da sua feitura? – Aqui está um espectáculo para quem se interessa por tudo que é importante na vida mas, muito especialmente, para quem se interessa por QUÍMICA e/ou MUSEOLOGIA.
O autor – Carl Djerassi – já esteve em Portugal, na Seiva Trupe, há 4 anos, assistindo a uma sua obra teatral – Oxigénio – que também foi um grande sucesso. Agora, Djerassi regressa ao n/ país para estar presente na estreia de FALÁCIA e nessa altura a Universidade do Porto irá nomeá-lo Doutor Honoris Causa, integrando o evento nas comemorações do Centenário da Universidade e no Ano Internacional da Química.
Espectáculo, também integrado nas comemorações do 70º Aniversário da Liga Portuguesa Contra o Cancro.
A direcção tem a assinatura de Júlio Cardoso.
Os cenários são da autoria do Professor José Carlos Barros e no elenco teremos António Reis, Clara Nogueira, Joana Esteves, Joana Estrela, Joel Sines e Jorge Loureiro.
Retirado de http://www.seivatrupe.pt/
Mas quem é Carl Djerassi?
Carl Djerassi nasceu em Viena, Áustria, em 29 de Outubro de 1923, mas foi educado nos Estados Unidos e tem nacionalidade norte-americana. Notabilizou-se como cientista na área da química, sendo conhecido, sobretudo, pelo seu decisivo contributo no desenvolvimento da pílula anticoncepcional. É também autor de uma importante obra literária, onde avultam peças de teatro, contos, poemas, novelas, textos memorialistas e uma autobiografia que ilustram o lado humano da ciência e os conflitos interiores que os cientistas enfrentam. Duas das suas peças, Oxigénio e Falácia, foram publicadas pela U. Porto Editorial.
Licenciado em Kenyon College (1942) e doutorado na Universidade de Wisconsin (1945), Djerassi possui uma longa e prestigiada carreira académica. É autor de mais de 1200 publicações científicas e de sete monografias, tendo sido galardoado com a National Medal of Science (em 1973, pela primeira síntese de um esteróide contraceptivo oral, a pílula) e com a National Medal of Technology (em 1991, por ter desenvolvido novas estratégias para o controlo de insectos).
Actualmente, é professor emérito de Química da Universidade de Stanford e membro da Academia Nacional das Ciências dos Estados Unidos e da Academia Americana das Artes e Ciências, assim como de várias academias estrangeiras.
Djerassi recebeu, por diversas vezes, o doutoramento honoris causa e foi distinguido com vários títulos honoríficos, de que se destacam: o primeiro Wolf Prize em Química (1978); o primeiro National Academy of Sciences Award for the Industrial Application of Science (1990); a Medal Priestley da American Chemical Society (1992); a Medalha Erasmus da Academia Europeia (2003); a Cruz de Grande Mérito da Alemanha (2003); a Medalha de Ouro do American Institute of Chemistry (2004); o Prémio Serono da Literatura (Roma, 2005); a Grande Condecoração em Prata por Serviços prestados à República da Áustria (2008); entre outras distinções. Em 2005, os correios austríacos editaram um selo em sua honra.
Carl Djerassi é o maior coleccionador privado de obras de Paul Klee e é fundador do Djerassi Resident Artists Program, na California.
(informação da Seiva Trupe)
sábado, 29 de outubro de 2011
Azeitonas recheadas... sim também podem ter alginato!
Se comprar um frasco de azeitonas verdes recheadas com pimento e olhar para a lista de ingredientes, possivelmente vai ler qualquer coisa como:
Ingredientes
Azeitonas verdes, pasta de pimento (25%), água, sal, reguladores de acidez: ácido láctico (E270), lactato de cálcio (E327), ácido cítrico (E330),antioxidante: ácido ascórbico (E300). Espessantes alginato de sódio (E401), Goma de guar (E412)
É que aquelas tirinhas não são de pimento que foi arranjado, cozinhado, cortado em tirinhas... não era viável... o que aconteceu é que foi feita uma pasta de pimento que foi texturizada com alginato, e ainda outro gelificante chamado goma guar, e com que foram feitas longas tiras que foram depois usadas para rechear as azeitonas. Tal foi feito de forma a que essas tiras de pasta de pimento tenham uma textura semelhante a um pimento em conserva. O sabor é o mesmo também.
E não se preocupe porque não faz mal nenhum à saúde. Já lhe dissémos que o alginato está aprovado para ser usado na alimentação e não se conhecem efeitos adversos se fôr usado nas doses adequadas.
sexta-feira, 28 de outubro de 2011
Esferificação inversa
Ao tipo de esferificação anteriormente (ontem) referida, chama-se esferificação directa, mas existe outro processo usado muitas vezes para as esferas de maiores dimensões – a esferificação inversa.
(imagem DAQUI)
Esta consiste em submergir um líquido rico em cálcio (como por exemplo iogurte) ou com este adicionado, num banho de alginato.
(imagem DAQUI)
Esta técnica, de grande versatilidade, permite uma preparação antecipada, assim como a realização de esferas com produtos com elevado teor em cálcio e produtos alcoólicos.
quinta-feira, 27 de outubro de 2011
Esferificação directa
Apesar dos alginatos serem muito usados pela indústria alimentar e de frequentemente ingerirmos alimentos com alginatos, o que tornou estas substâncias "famosas" foi a sua utilização na cozinha por Ferran Adrià, chefe do restaurante El Bulli na Catalunha.
Usando a propriedade dos alginatos de gelificar em presença de cálcio, Ferran Adrià desenvolveu uma técnica culinária a que chamou esferificação.
A “esferificação” permite a elaboração de pequenas esferas com qualquer líquido. Para tal basta dissolver alginato no líquido que se pretende esferificar e deixar cair este (a técnica usada para isso depende do tamanho das esferas desejadas) numa solução rica em cálcio. Forma-se imediatamente uma película externa gelificada, que contém o líquido no seu interior. A este tipo de esferificação chama-se "esferificação directa".
Esta técnica permite obter esferas de diferentes tamanhos: "caviares" (esferas de pequenas dimensões) até esferas de maiores dimensões, do tamanho de gemas de ovo, podendo introduzir-se ainda elementos sólidos dentro destas.
Estas esferas devem contudo ser preparadas apenas na altura de servir, sobretudo as de menores dimensões, pois o cálcio migra para o interior e ao fim de alguns minutos toda a esfera está sólida, perdendo-se bastante o sabor do líquido que foi esferificado.
Usando a propriedade dos alginatos de gelificar em presença de cálcio, Ferran Adrià desenvolveu uma técnica culinária a que chamou esferificação.
A “esferificação” permite a elaboração de pequenas esferas com qualquer líquido. Para tal basta dissolver alginato no líquido que se pretende esferificar e deixar cair este (a técnica usada para isso depende do tamanho das esferas desejadas) numa solução rica em cálcio. Forma-se imediatamente uma película externa gelificada, que contém o líquido no seu interior. A este tipo de esferificação chama-se "esferificação directa".
Esta técnica permite obter esferas de diferentes tamanhos: "caviares" (esferas de pequenas dimensões) até esferas de maiores dimensões, do tamanho de gemas de ovo, podendo introduzir-se ainda elementos sólidos dentro destas.
Estas esferas devem contudo ser preparadas apenas na altura de servir, sobretudo as de menores dimensões, pois o cálcio migra para o interior e ao fim de alguns minutos toda a esfera está sólida, perdendo-se bastante o sabor do líquido que foi esferificado.
quarta-feira, 26 de outubro de 2011
Os alginatos que as algas nos dão
Os alginatos são hidratos de carbono (polissacáridos - moléculas longas formadas pela interligação de moléculas de açúcares simples) que se extraem de algumas algas castanhas, Phaeophyceae.
Estas algas produzem uma mistura de vários sais do ácido algínico, os alginatos, que são uma componente das suas células que confere aos organismos muita flexibilidade e que são a matéria prima base para a produção industrial de alginatos.
Os alginatos têm uma grande variedade de aplicações devido às suas propriedades de:
-retenção da água;
-gelificantes;
-espessantes;
-estabilizantes.
Para a formação de géis (redes tridimensionais que retêm a água no interior) as cadeias dos alginatos ligam-se entre si na presença de iões cálcio.
Os alginatos são usados em cosmética, na indústria farmacêutica e na indústria alimentar, neste caso, por exemplo, como estabilizantes, espessantes ou agentes gelificantes em molhos, sobremesas, gelados, produtos cárneos e produtos reconstituídos da batata.
De facto, o ácido algínico e os alginatos fazem parte dos aditivos alimentares permitidos pela legislação comunitária europeia, conhecidos pela designação de E’s. São todos considerados inofensivos e alguns (E400, E401, E402) são mesmo admitidos em alimentos certificados como biológicos e em alimentos destinados a bebés.
Estas algas produzem uma mistura de vários sais do ácido algínico, os alginatos, que são uma componente das suas células que confere aos organismos muita flexibilidade e que são a matéria prima base para a produção industrial de alginatos.
Os alginatos têm uma grande variedade de aplicações devido às suas propriedades de:
-retenção da água;
-gelificantes;
-espessantes;
-estabilizantes.
Para a formação de géis (redes tridimensionais que retêm a água no interior) as cadeias dos alginatos ligam-se entre si na presença de iões cálcio.
Os alginatos são usados em cosmética, na indústria farmacêutica e na indústria alimentar, neste caso, por exemplo, como estabilizantes, espessantes ou agentes gelificantes em molhos, sobremesas, gelados, produtos cárneos e produtos reconstituídos da batata.
De facto, o ácido algínico e os alginatos fazem parte dos aditivos alimentares permitidos pela legislação comunitária europeia, conhecidos pela designação de E’s. São todos considerados inofensivos e alguns (E400, E401, E402) são mesmo admitidos em alimentos certificados como biológicos e em alimentos destinados a bebés.
terça-feira, 25 de outubro de 2011
O calendário de Outubro fala-nos de um tipo de medicamentos muito útil...
O tema do calendário de Outubro está relacionado com a saúde. É uma oportunidade de aprender mais sobre antibióticos...
The Chemistry Calendar for the
International Year of Chemistry 2011
Outubro
segunda-feira, 24 de outubro de 2011
Polifenol oxidase - aprenda como lidar com ela!
Nota: O video que tinhamos inicialmente deixou de estar disponível, pelo que o substituimos por um outro.
domingo, 23 de outubro de 2011
A Química na Arte XXVI

Mas tal como numa molécula a troca de um ou dois átomos pode fazer uma diferença significativa nas suas características e funções... também a troca de uma ou duas letras quando se faz uma busca para encontrar uma molécula pode levar a que se encontre outra...
Na capa do single, por baixo de uma estrutura de uma molécula aparece uma legenda descrevendo o que é e que funções tem a Melanina - pigmentos insolúveis, presentes no reino animal responsáveis pela côr escura da pele e cabelos...
Mas quando foram procurar a molécula, procuraram Melamina e é deste composto a estrutura molecular que ilustra a capa do single... que tem propriedades de retardador de fogo, devido a libertar azoto quando arde, e tem vários outras aplicações industriais como por exemplo ser usado na produção de resinas de melamina (usada em fórmicas, loiças de plástico...).
sábado, 22 de outubro de 2011
Fermentação Maloláctica
A fermentação maloláctica é um processo usado na produção de vinho, em que o ácido málico, naturalmente presente no mosto, e com um gosto ácido um pouco agressivo, é convertido em ácido láctico, com um tipo de acidez mais suave. O ácido málico tem um sabor a maçãs verdes. Por outro lado, o ácido láctico tem um sabor mais rico e amanteigado.
As uvas produzidas em regiões frias tendem a ter uma elevada acidez que muito se deve à contribuição de ácido málico.
A fermentação maloláctica contribui para acrescentar complexidade e delicadeza aos vinhos que a ela são submetidos (há tipos de vinho para os quais não é indicada) resultando em vinhos mais equilibrados, redondos e harmoniosos…
As uvas produzidas em regiões frias tendem a ter uma elevada acidez que muito se deve à contribuição de ácido málico.
A fermentação maloláctica contribui para acrescentar complexidade e delicadeza aos vinhos que a ela são submetidos (há tipos de vinho para os quais não é indicada) resultando em vinhos mais equilibrados, redondos e harmoniosos…
sexta-feira, 21 de outubro de 2011
Ervilhas congeladas
As ervilhas quando são apanhadas têm um conteúdo alto de açúcar e são docinhas e muito saborosas. No entanto, assim que são apanhadas, os açúcares começam a converter-se em amido, que não é doce e dá uma textura diferente. Algumas horas depois de serem apanhadas, já são menos boas, alguns dias depois, não têm graça nenhuma, ficam duras e com pouco sabor. É o metabolismo normal das ervilhas e só há uma forma de evitar as reacções químicas que transformam os açúcares em amido - manter a temperatura baixa, retarda-as, congelar praticamente impede que ocorram.
Quem tem uma plantação de ervilhas ao pé, as colhe, descasca e mete no tacho tem as ervilhas no seu melhor. Quem as obtém só alguns dias depois de colhidas, e sobretudo se não estiveram armazenadas a temperatura adequada, não pode ter as ervilhas no seu melhor. Por esta razão uma percentagem muito baixa das ervilhas são vendidas frescas (cerca de 5%), tudo o resto é vendido enlatado (mas têm pouca graça) ou congelado. As grandes empresas, de forma a obter um produto com a maior qualidade possível, congelam as ervilhas muito pouco tempo depois de terem sido colhidas (poucas horas) de forma ao produto ser o mais semelhante possível a ervilhas acabadas de colher. E com processos de congelação muito rápidos e usando técnicas muito sofisticadas.
Da próxima vez que fôr ao supermercado repare que os pacotes de ervilhas congeladas têm a informação de que elas foram congeladas poucas horas depois de terem sido colhidas, é uma forma de lhe indicar que são o melhor que pode ter.
Quem tem uma plantação de ervilhas ao pé, as colhe, descasca e mete no tacho tem as ervilhas no seu melhor. Quem as obtém só alguns dias depois de colhidas, e sobretudo se não estiveram armazenadas a temperatura adequada, não pode ter as ervilhas no seu melhor. Por esta razão uma percentagem muito baixa das ervilhas são vendidas frescas (cerca de 5%), tudo o resto é vendido enlatado (mas têm pouca graça) ou congelado. As grandes empresas, de forma a obter um produto com a maior qualidade possível, congelam as ervilhas muito pouco tempo depois de terem sido colhidas (poucas horas) de forma ao produto ser o mais semelhante possível a ervilhas acabadas de colher. E com processos de congelação muito rápidos e usando técnicas muito sofisticadas.
Da próxima vez que fôr ao supermercado repare que os pacotes de ervilhas congeladas têm a informação de que elas foram congeladas poucas horas depois de terem sido colhidas, é uma forma de lhe indicar que são o melhor que pode ter.
quinta-feira, 20 de outubro de 2011
Uma descoberta que marcou muitas sociedades
Nos anos 1930's, em resultado do trabalho de um conjunto de cientistas, compreendeu-se que uma mulher não podia ficar grávida se os níveis de estrogénio e progesterona no seu organismo ultrapassassem determinados valores. Estes dois esteróides (assim se chama o grupo de moléculas a que pertencem) impedem que o organismo produza hormonas importantes para que se dê a ovulação. Este conhecimento levou a que se pusesse a hipótese de que seria possível, administrando estes esteróides, controlar artificialmente a fertilidade.
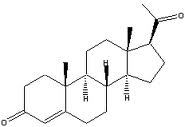
A empresa alemã Schering Laboratories demonstrou grande interesse sobre este assunto e a sua aplicação comercial. Nos seus laboratórios isolaram, em 1934, 20 mg de progesterona natural de 625 kg de ovários obtidos de 50.000 porcas. Apesar de ser um feito remarcável, isto demonstrava também como era difícil e economicamente inviável obter a progesterona.por este processo A dificuldade em obter esta substância fez com que o projecto tivesse que ser adiado.
Em 1941, o químico Russel E. Marker, da Pennsylvania State University (USA) descobriu uma forma de sintetizar progesterona, partindo de uma substância chamada diosgenina extraída de plantas. Na altura não conseguiu que a empresa Parke-Davis, com quem colaborava, se interessasse suficientemente pelo assunto e foi para o México (tinha descoberto que uma espécia de inhame mexicano era muito rico em diosgenina), onde criou a sua própria empresa, Syntex, para produzir progesterona e outros esteróides.
No entanto, o marco decisivo no processo de desenvolvimento dos contraceptivos orais ocorreu quando o químico Carl Djerassi mais tarde, também na empresa Syntex, sintetizou um outro esteróide a que se chamou noretindrona e que se verificou ser oito vezes mais potente que a progesterona e, ainda mais importante do que isso, activo se tomado oralmente.
Na altura já vários grupos de investigação, em paralelo, trabalhavam na síntese e teste de esteróides com vista à criação de um contraceptivo oral e foi concluído que a "pílula" era um processo eficiente de controle da natalidade. Foi então submentido à Food and Drug Administration (FDA), nos USA, um medicamento chamado Enovid com este propósito. Este foi aprovado, inicialmente apenas para o tratamento de problemas de saúde, já que a contracepção era um assunto muito controverso. Finalmente, no início dos anos 1960, a situação mudou, já que na prática muitas mulheres já tomavam o Enovid como contraceptivo. Nos anos que se seguiram a formulação da pílula mudou, tornando-a mais eficiente e com menos efeitos secundários.
Esta foi uma descoberta que mudou radicalmente muitas sociedades por todo o mundo e que foi uma contribuição decisiva para a emancipação da mulher.
A empresa alemã Schering Laboratories demonstrou grande interesse sobre este assunto e a sua aplicação comercial. Nos seus laboratórios isolaram, em 1934, 20 mg de progesterona natural de 625 kg de ovários obtidos de 50.000 porcas. Apesar de ser um feito remarcável, isto demonstrava também como era difícil e economicamente inviável obter a progesterona.por este processo A dificuldade em obter esta substância fez com que o projecto tivesse que ser adiado.
Em 1941, o químico Russel E. Marker, da Pennsylvania State University (USA) descobriu uma forma de sintetizar progesterona, partindo de uma substância chamada diosgenina extraída de plantas. Na altura não conseguiu que a empresa Parke-Davis, com quem colaborava, se interessasse suficientemente pelo assunto e foi para o México (tinha descoberto que uma espécia de inhame mexicano era muito rico em diosgenina), onde criou a sua própria empresa, Syntex, para produzir progesterona e outros esteróides.
progesterona
No entanto, o marco decisivo no processo de desenvolvimento dos contraceptivos orais ocorreu quando o químico Carl Djerassi mais tarde, também na empresa Syntex, sintetizou um outro esteróide a que se chamou noretindrona e que se verificou ser oito vezes mais potente que a progesterona e, ainda mais importante do que isso, activo se tomado oralmente.
noretindrona
Na altura já vários grupos de investigação, em paralelo, trabalhavam na síntese e teste de esteróides com vista à criação de um contraceptivo oral e foi concluído que a "pílula" era um processo eficiente de controle da natalidade. Foi então submentido à Food and Drug Administration (FDA), nos USA, um medicamento chamado Enovid com este propósito. Este foi aprovado, inicialmente apenas para o tratamento de problemas de saúde, já que a contracepção era um assunto muito controverso. Finalmente, no início dos anos 1960, a situação mudou, já que na prática muitas mulheres já tomavam o Enovid como contraceptivo. Nos anos que se seguiram a formulação da pílula mudou, tornando-a mais eficiente e com menos efeitos secundários.
Esta foi uma descoberta que mudou radicalmente muitas sociedades por todo o mundo e que foi uma contribuição decisiva para a emancipação da mulher.
quarta-feira, 19 de outubro de 2011
Amino-ácidos essenciais
Já aqui lhe falámos de proteínas e dissemos que eram longas moléculas formadas por unidades mais pequenas, os amino-ácidos, ligadas entre si. Também lhe dissémos que há 20 amino-ácidos que são a base das proteínas de todos os organismos vivos.
(grupos amina e ácido carboxílico, que dão o nome a este grupo de moléculas, dentro de círculos; o grupo R é o que distingue os aminoácidos uns dos outros)
Na figura anterior, os amino-ácidos assinalados com uma seta vermelha são aqueles a que se chama amino-ácidos essenciais. Estes são amino-ácidos que o organismo considerado (normalmente, o humano) não é capaz de sintetizar mas são fundamentais para o seu funcionamento.
O organismo humano é incapaz de sintetizar cerca de metade dos vinte amino-ácidos comuns. Tem então que os obter através da dieta, pela ingestão de alimentos ricos em proteínas que os contenham.
Os aminoácidos não essenciais são também necessários para o funcionamento do organismo, mas podem ser sintetizados in vivo.
Alimentos de origem animal, como carne, peixes, ovos e leite são consideradas fontes de proteínas completas, pois estas contêm todos os amino ácidos essenciais. Já nos alimentos de origem vegetal isso não acontece, Daí a importância de variar a dieta e misturar várias fontes de proteínas.
Dietas vegetarianas muito rigorosas exigem cuidados especiais, como misturar sempre legumes e cereais variados de forma a que, em conjunto, forneçam de forma equilibrada os amino-ácidos essenciais. Curiosamente,combinações comuns na alimentação tradicional de alguns povos, como por exemplo o arroz com feijão na América do Sul, são formadas por alimentos em que os amino-ácidos presentes se complementam para fornecer ao organismo todos os amino-ácidos essenciais.
Dietas vegetarianas muito rigorosas exigem cuidados especiais, como misturar sempre legumes e cereais variados de forma a que, em conjunto, forneçam de forma equilibrada os amino-ácidos essenciais. Curiosamente,combinações comuns na alimentação tradicional de alguns povos, como por exemplo o arroz com feijão na América do Sul, são formadas por alimentos em que os amino-ácidos presentes se complementam para fornecer ao organismo todos os amino-ácidos essenciais.
terça-feira, 18 de outubro de 2011
Transformar plásticos em petróleo, gasolina ou diesel
Há umas semanas um dos nossos leitores enviou-nos um email em que dizia:
Caras químicas e caros químicos,
Acompanho desde há alguns meses o vosso interessante e útil blog e muitas respostas já obtive a questões que permaneciam escondidas e que assim saíram cá para fora, de repente... Parabéns e continuem...
Esta semana fui literalmente assediado por umas amigas que queriam convencer-me que um japonês,
imaginem... tinha inventado uma engenhoca que transformava plásticos em petróleo, gasolina ou diesel a pedido... coisas da net... aliás o video promocional é de uma entidade que se intitula "United Nations University"...
Fui ver e... eis que na América também há quem se interesse por essas tecnologias...
Não pesquisei toda informação já presente no vosso blog, onde este assunto até poderá ter sido comentado...
Eis um tema que gostaria de ver abordado, na generalidade, sendo esta situação apenas uma curiosidade...
Aqui fica o referido vídeo:
Pusémos a questão à Professora Ana Ramos da FCT/UNL que nos disse:
Caras químicas e caros químicos,
Acompanho desde há alguns meses o vosso interessante e útil blog e muitas respostas já obtive a questões que permaneciam escondidas e que assim saíram cá para fora, de repente... Parabéns e continuem...
Esta semana fui literalmente assediado por umas amigas que queriam convencer-me que um japonês,
imaginem... tinha inventado uma engenhoca que transformava plásticos em petróleo, gasolina ou diesel a pedido... coisas da net... aliás o video promocional é de uma entidade que se intitula "United Nations University"...
Fui ver e... eis que na América também há quem se interesse por essas tecnologias...
Não pesquisei toda informação já presente no vosso blog, onde este assunto até poderá ter sido comentado...
Eis um tema que gostaria de ver abordado, na generalidade, sendo esta situação apenas uma curiosidade...
Aqui fica o referido vídeo:
Pusémos a questão à Professora Ana Ramos da FCT/UNL que nos disse:
Não é engenhoca nem ficção: É a pirólise de resíduos dos plásticos de maior consumo mundial, polietileno, polipropileno e poliestireno (o PVC fica de fora por causa do cloro), em atmosfera inerte e entre 300 e 400ºC, que vai dar origem a misturas de hidrocarbonetos que podem ser utilizadas como combustíveis ou matéria prima para a indústria petroquímica. Esse trabalho de investigação é também realizado em Portugal no INETI, actualmente LNEG (Laboratório Nacional de Energia e Geologia, no Laboratório de Emissões Zero). Já lá foram realizadas duas teses de doutoramento, já concluídas, sobre esse assunto e há outra em curso sobre pirólise de plásticos e biomassa. Existem algumas unidades industriais no mundo, mas ainda muito poucas, porque estamos a falar de indústria química pesada, com investimentos muito elevados e o outro problema que ainda se coloca é o da recolha selectiva de resíduos.
Só mais uma curiosidade: esse processo chama-se reciclagem química de materiais plásticos. Existe a
reciclagem mecânica que é a mais comum, não envolve qualquer transformação química, apenas o novo processamento de materiais reciclados em novos objectos de menor valor, p.e. as embalagens alimentares de polietileno, que são lavadas e granuladas, e essa nova matéria prima transformada em sacos de lixo.
Só mais uma curiosidade: esse processo chama-se reciclagem química de materiais plásticos. Existe a
reciclagem mecânica que é a mais comum, não envolve qualquer transformação química, apenas o novo processamento de materiais reciclados em novos objectos de menor valor, p.e. as embalagens alimentares de polietileno, que são lavadas e granuladas, e essa nova matéria prima transformada em sacos de lixo.
Agradecemos a ambos!
segunda-feira, 17 de outubro de 2011
A cebola, as lágrimas e outras coisas...
Clique nas imagens para as ver maiores
De "A Cozinha é um Laboratório" - Margarida Guerreiro e Paulina Mata
domingo, 16 de outubro de 2011
sábado, 15 de outubro de 2011
Se fazer leite creme lhe causa insegurança...
Vamos dar-lhe umas “dicas” para aumentar a sua probabilidade de sucesso quando fizer leite-creme.
Um passo fundamental na preparação desta deliciosa sobremesa é a desnaturação das proteínas das gemas do ovo. Ou seja, as proteínas, que no ovo se encontravam inicialmente na forma de novelos, desenrolam-se e começam a estabelecer novas ligações entre si, forma-se uma rede que retém o líquido no seu seio - um gel (no caso do leite-creme o líquido é o leite com o açúcar e todos os aromas que lhe introduzimos).
Mas se essas ligações forem em grande número, a rede torna-se demasiado apertada e acaba por expulsar parte do líquido. Há que evitá-lo a todo o custo!
A coagulação das proteínas das gemas inicia-se aos 65ºC; mas com o leite essa temperatura passa para valores mais altos - cerca de 82ºC – porque elas ficam diluídas e mais separadas. Por segurança, não se deve deixar que a temperatura do preparado ultrapasse os 80ºC. Na prática, isso significa que está pronto quando cobre com uma fina camada as costas duma colher de pau.
Caso, para fazer o seu leite creme, use apenas leite ovos e açúcar, a textura vai apenas depender da coagulação das proteínas do leite e será necessária alguma experiência e muita, muita atenção. É que num segundo está tudo bem e no seguinte o leite-creme pode ficar todo “talhado”, ou seja, uma massa dos ovos demasiado cozidos para um lado e o leite para outro. Em cima do lume corre-se o risco de ser difícil controlar o aquecimento, uma vez que há sempre zonas do tacho que aquecem mais e, nessas, as proteínas ligam-se muito umas às outras. Nesse caso, lá se vai o nosso leite-creme. Depois… não há remédio. O ideal é engrossar o leite-creme em banho-maria, o que permite controlar melhor a temperatura que o preparado vai atingindo ou, como alternativa, usar um tacho de fundo espesso, que permita uma boa distribuição do calor.
Se decidir juntar uma colherzinha de farinha maizena, o processo fica bastante facilitado. Sem a maizena a 82ºC lá se ia o leite-creme, com a maizena o preparado não começou sequer a engrossar. Isto significa que com muita segurança pode fazer o leite-creme directamente em cima do lume sem necessitar de banho-maria.
E como é que uma quantidade tão pequena de maizena faz este efeito? Não se sabe ainda bem, mas provavelmente as proteínas desnaturadas dos ovos não se ligam umas às outras com a mesma facilidade. O amido expande e gelatiniza e vai-se meter entre as proteínas, constituindo assim uma barreira física que dificulta as ligações entre elas. Desta forma leite-creme não talha tão facilmente. É verdade que também não fica tão bom como um leite creme sem farinha, mas fica bem melhor do que um leite creme "talhado"... a decisão é sua.
sexta-feira, 14 de outubro de 2011
quinta-feira, 13 de outubro de 2011
Post-it
Em 1968, Spencer F. Silver, um químico da 3M a trabalhar em adesivos sensíveis à pressão, descobriu que quando um co-polímero de acrilato era produzido de umas determinada forma, se formava uma suspensão de microesferas ligadas entre si. As microesferas não se dissolviam em solução, de facto inchavam até duplicar o seu diâmetro original. Quando esta mistura era pulverizada numa dada superfície, o solvente evaporava e as microesferas voltavam ao seu tamanho original.
Assim, ao contrário de outros adesivos que formavam uma superfície plana contínua, este formava uma superfície descontínua, parecida com a de uma bola de basquete.
Na altura a 3M não sabia o que fazer com este tipo de adesivo, mas foi considerado que ele tinha potencial para ser usado no desenvolvimento de novos produtos.
Na altura a 3M não sabia o que fazer com este tipo de adesivo, mas foi considerado que ele tinha potencial para ser usado no desenvolvimento de novos produtos.
Em 1974 Art Fry, um engenheiro químico da 3M, estava a cantar no coro da igreja quando, de repente, teve a ideia de que um marcador removível seria de grande utilidade. Lembrou-se de cola de Silver e, em 1980, o Post-it nasceu.
A superfície irregular do adesivo de microesferas só permite um número limitado de pontos de contacto entre o Post-it e a superfície onde é colado, o que faz com que possa ser removido e colado de novo.
Adaptado de: http://pubs.acs.org/cen/whatstuff/stuff/8214sci3.html
E aqui ficam dois presentes...
Retirado daqui: http://thingsweforget.blogspot.com/
Um blog que vale mesmo a pena visitar!
quarta-feira, 12 de outubro de 2011
Bolos mais leves
Sabia que numa receita de um bolo que leva gordura, por exemplo manteiga, pode substituí-la por purés de frutos ou vegetais ricos em pectina para o tornar mais leve?
Os purés de maçã ou cenouras, por exemplo, mimetizam o papel desempenhado pela gordura para tornar os bolos mais macios e agradáveis. A sua pectina dificulta a formação do glúten (uma rede formada por proteínas da farinha de trigo), de uma forma idêntica ao que acontece com a gordura. Por outro lado, a água dos purés contribui para tornar o bolo mais húmido.
Os bolos que se obtêm substituindo a gordura por purés ricos em pectina são, contudo, mais densos do que os levam gordura. Para uma boa textura e um bolo menos calórico, o ideal é usar misturas de gordura e puré. Por exemplo, substituir ½ chávena de manteiga por ¼ de chávena de manteiga e ¼ de chávena de puré de fruta.
terça-feira, 11 de outubro de 2011
Velas mágicas
Imagine uma festa de aniversário… o aniversariante sopra as velas do seu bolo de aniversário, apagam-se… mas… de repente, as chamas reaparecem… e por muitas que sejam as tentativas para as apagar, a velas teimam em reacender. Velas mágicas!
O segredo? Já está a imaginar que tem a ver com química…
As velas são feitas de cera, o combustível da vela. O pavio frequentemente de algodão é tratado com uma solução de um sal para evitar que seja destruído muito rapidamente pelas chamas.
Nas velas mágicas, incorpora-se pó de magnésio no pavio. O magnésio é um metal altamente reactivo, quando está em pó e inflama-se a temperaturas relativamente baixas (430 º C). Quando a chama se apaga, calor do pavio inflama o pó de magnésio, produzindo faíscas minúsculas. Estas, por sua vez, inflamam a cera que ainda está sob a forma de vapor, o que reacende o pavio. O magnésio mais abaixo no pavio não se queima, porque está protegido pela cera.
É preciso contudo ter cuidado com estas velas devido pois o que nos diverte nelas, pode também ser a causa de incêndio se não se tiver cuidado.
segunda-feira, 10 de outubro de 2011
Já alguma vez pensou como funciona uma vela?
Olhemos para uma vela atentamente… ela contém duas partes distintas:
- Uma componente feita com um qualquer tipo de cera
- Um pavio, feito com uma fibra.
Estas duas componentes são fundamentais e cada uma desempenha um papel diferente.
Comecemos pela cera, frequentemente é cera de parafina (hidrocarbonetos obtidos a partir do petróleo). É, de facto, um combustível sólido.
Quanto ao pavio este tem que ser fabricado com um material muito absorvente. Tal é importante porque o pavio precisa absorver cera líquida para que ela suba sempre enquanto a vela estiver acesa. Já vamos ver a razão…
Quando se acende uma vela, o calor do fósforo, derrete a cera que está no pavio e a que está à volta dele. O calor da chama evapora a cera e é o vapor da cera que se queima. Sendo o pavio absorvente, à medida que a cera vai vaporizando, mais cera líquida vai subindo por capilaridade e ali, com o calor da chama é suficiente para ir derretendo mais cera, liquefazendo-a, cera esta que vai, por capilaridade, subir. Com o calor esta cera no pavio vai-se vaporizar e é a cera no estado gasoso que vai manter a vela acesa. Esta é de facto uma reacção em cadeia auto-sustentável.
Subscrever:
Comentários (Atom)