Não sou uma pessoa muito observadora.
Tenho pena, porque há coisas interessantes que me escapam completamente.
Há uns anos, num pequeno almoço num hotel em Copenhaga, disseram-me "Já
reparaste que o mel é cremoso e que dá para barrar?". Não, não tinha
reparado... E a pergunta seguinte foi "O que é que eles adicionarão ao
mel para ficar assim?". Não sabia, mas fiquei com curiosidade. Não fosse
dar jeito... meti 2 ou 3 doses de mel na carteira. Foi a minha sorte!
A Patrícia de vez em quando diz "O
google é o nosso melhor amigo." E tenho que lhe dar alguma razão.
Cheguei, googlei e logo descobri que era apenas mel que tinha sido
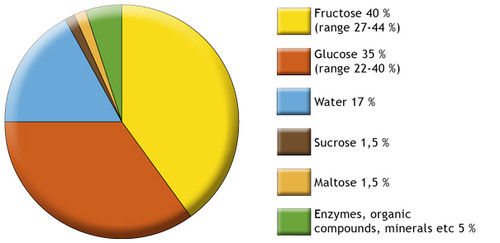
cristalizado. De facto, o mel é uma solução sobressaturada de açúcar, em
geral mais de 70% de açúcar e menos de 20% de água, e sendo assim é
instável. Por isso frequentemente cristaliza.
Os principais açúcares no mel são a
frutose e a glucose, em geral um pouco mais de frutose do que de
glucose. O açúcar que cristaliza é a glucose, pois a sua solubilidade em
água (910 g/L a 25 ºC) é menor que a da frutose (3750 g/L a 20 ºC),
sendo esta mais difícil de cristalizar.
Ainda há dias fui dar com uma embalagem
de um mel que quando comprei era fluido e agora, com o tempo mais frio,
tinha cristalizado. Quando isto acontece o mel pode ficar menos
agradável de comer, se os cristais forem grandes vão tornar o mel
arenoso. No entanto, se os cristais forem muito pequenos, o mel fica
transformado num creme com uma textura muito agradável, e que dá para
barrar. Tem ainda a vantagem de não se sujar tudo à volta com pingos de
mel.
O que fazem alguns produtores de mel, é
cristalizarem o mel de forma controlada, de modo a se formarem muitos
cristais pequenos, obtendo um mel que muita gente prefere por ser
igualmente saboroso e mais fácil de usar. Um processo há muito usado, a
patente foi registada em 1935 por Elton J. Dyce. Era assim que aquele
mel era produzido, nada lhe tinha sido adicionado. Tinha apenas sido
cristalizado.
Googlando encontrei logo instruções para
fazer este mel cremoso. Bastava misturar bem 10% do melhor mel cremoso
que encontrasse, com 90% do mel fluido que desejava cristalizar, pôr em
lugar fresco e esperar. Os cristais que se adicionam induzem a
cristalização e vão determinar a forma dos cristais que se vão formar.
Assim fiz, usando os pacotinhos que tinha trazido de Copenhaga. Coloquei
num local fresco e duas semanas depois tinham um frasco de mel cremoso.
Uns dias depois no supermercado, vi que há à venda mel cremoso produzido cá pela
SerraMel.
Um óptimo mel cremoso de flores de laranjeira. Saboroso e com uma
óptima textura, bem sedosa. É esse que uso agora quando quero um bom mel
cremoso.
Gráfico com a composição do mel DAQUI
Post inicialmente publicado no blog Assins & Assados